

F203 腺苷、腺嘌呤
一、化学结构与理化性质
腺苷(adenosine)又称腺嘌呤核苷、阿糖腺苷,化学名为9-β-D-呋喃核糖基腺嘌呤,分子式为C10H13N5O4,分子量为267.28,CAS号为58-61-7。
腺嘌呤(adenine)又称腺素、维生素B4,化学名为6-氨基嘌呤,分子式为C5H5N5,分子量为135.14,CAS号为73-24-5。
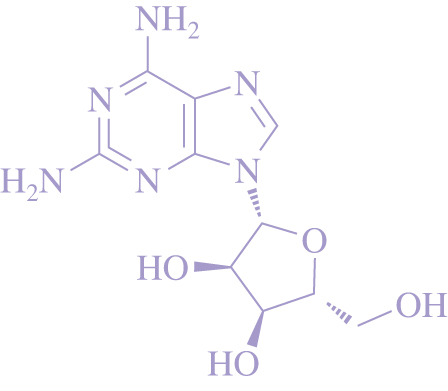
腺苷(腺嘌呤核苷)的化学结构
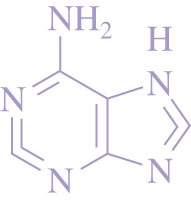
腺嘌呤的化学结构
腺苷为白色或类白色结晶性粉末,微有咸苦味,易溶于水,不溶于乙醇和乙醚,熔点233~238℃,比旋度-68°~-72°。水解得到腺嘌呤和D-核糖,脱氨基产生肌苷,于100℃真空处理失去结晶水。
腺嘌呤为白色针状结晶,具有强烈的咸味。220℃开始升华,360~365℃分解。1g腺嘌呤可溶于2 000ml水和40ml沸水,水溶液呈中性。溶于酸和碱,微溶于醇,不溶于醚及氯仿。
二、主要来源与生产制备方法
主要来源 腺苷是一种内源性的核苷酸,广泛存在于人和动物的组织细胞中,冬虫夏草中含量很高。腺嘌呤是存在于大多数生物体内的4种含氮碱基之一,其主要存在的植物有竹叶和桑叶、紫云英、茄、平车前和车前的种子、南瓜以及菌类,如茯苓的菌核、香蕈、墨汁鬼和中国南海海绵等。
生产制备方法 工业上主要通过离子交换法、微波萃取法等分离提取腺苷,或以肌苷为原料,通过乙酰化、氯化、氨解得到腺苷(收率≥50%)或通过功能基团转换制备腺苷(收率约62%),还可以次黄嘌呤为原料利用微生物发酵生产腺苷(收率约90%),平均产量为7~8g/L。
腺嘌呤主要以氨基丙二脒双盐酸和二甲基甲酰胺为原料制取或作为谷氨酸发酵过程的副产品回收得到。腺嘌呤可由酵母核酸先提取出腺嘌呤核苷酸,再经酸水解而获到,也可经多种化学方法合成,如用甲脒和丙二腈的偶氮苯为原料,也可高产率地获得腺嘌呤。
三、分析方法
GB 未查见相关标准。
AOAC 未查见相关标准。
其他 目前,用于分析腺苷的方法有高效液相色谱法(HPLC)(美国药典USP28)、HPLC-MS[1]、薄层色谱-紫外分光光度法(TLC-UV)[2]、胶束电动色谱(micellar electrokinetic chromatogaraphy)[3],毛细管电泳法[4]等方法。
腺嘌呤的分析方法包括化学修饰电极方法[5]、化学发光方法[6]和吸附溶出伏安法[7]等。
四、生理功能及作用
内源性神经递质 腺苷可减慢房室结节的传导时间,并通过房室结节阻断回路途径,恢复阵发性室上性心动过速(PSVT),甚至可恢复PSVT与Wolff-Parkinson-While综合征患者的正常窦性心律[8]。可直接进入心肌经磷酸化生成腺苷酸,参与心肌能量代谢,同时还参与扩张冠状动脉,增加血流量。
抗缺氧作用 腺苷还具有增加血红蛋白和2,3-二磷酸甘油含量的作用,可增强血液供氧能力和加速血液微循环,提高血液对心、脑的供氧能力。
其他 其片剂或注射剂用于防治各种原因引起的白细胞减少症,特别是由于肿瘤化疗、放射治疗及苯类等药物中毒所造成的白细胞减少。
五、安全性研究
1、人群资料
腺苷[9]:女性静脉给药的最低中毒剂量(TDLo)为240μg/kg,表现为心律失常;男性静脉给药的TDLo为143μg/kg,表现为对感官和眼睛的影响和头疼。
腺嘌呤:尚未查阅到相关资料。
2、代谢情况 静脉注射腺苷可迅速被细胞(主要指红细胞和血管内皮细胞)吸收,半衰期约为10s。
3、急性毒性
腺苷:大鼠经口染毒LD50>20 000mg/kg,小鼠腹腔注射LD50为500mg/kg[9]。
腺嘌呤:大鼠经口染毒LD50,为227mg/kg,腹腔注射LD50为198mg/kg,表现为惊厥、肌无力、发绀和睡眠时间改变等。小鼠经口染毒LD50为783mg/kg,腹腔注射LD50为100mg/kg,静脉注射LD50>300mg/kg,皮下最低致死剂量(LDLo)为1 000mg/kg[10]。
4、遗传毒性
腺苷:大肠埃希菌噬菌体抑制试验阳性(1 000mg/L),人体细胞基因突变试验阳性(0.1mmol/L),小鼠腹腔细胞遗传学试验(cytogeneticanalysis)阳性(178mg/kg),哺乳动物淋巴细胞DNA损伤试验阳性(60mmol/L)[9]。
腺嘌呤:大肠埃希菌噬菌体抑制试验阳性(1 000mg/L),人淋巴细胞性染色体丢失和试验(sex chromosome loss andnondisjunction test)阳性(2.5mmol/L),小鼠细胞遗传学试验阳性(经口250mg/kg和腹腔注射451mg/kg),小鼠精子形态(sperm morphology)试验异常(腹腔注射500mg/kg,连续给药5天[10]。
5、亚慢性毒性
腺苷:未查见相关文献资料。
腺嘌呤:大鼠亚慢性经口染毒最低中毒剂量为70mg/kg,表现为膀胱重量和白细胞计数发生改变,出现体重减低或增重下降。大鼠亚慢性经口最低中毒剂量为9 450mg/kg,也表现为体重减低或增重下降。大鼠腹腔注射最低中毒剂量为400mg/kg,表现为腹膜炎等。狗静脉注射最低中毒剂量为525mg/kg,表现为急性肾衰竭和肾小管坏死[10]。
6、慢性毒性与致癌性 未查见相关文献资料。
7、生殖与发育毒性
腺苷:未查见相关文献资料。
腺嘌呤[10]:雄性大鼠经口染毒的最低生殖毒性中毒剂量为5 040mg/kg(交配前染毒4周),表现为对睾丸、附睾和输精管的毒性作用。雌性大鼠腹腔注射最低生殖毒性中毒剂量为300mg/kg(受孕后10~12天),表现为胚胎眼部和耳朵或泌尿生殖系统发育异常。雌性小鼠腹腔最低生殖毒性剂量为200mg/kg(受孕后9~10天),表现为胎儿发育迟缓或死胎、胃肠道发育异常。雄性小鼠腹腔注射最低生殖毒性中毒剂量为500mg/kg(交配前5天染毒),表现为精子生成障碍、形态及运动异常、数量减少。
其他 未查见相关文献资料。
六、常见使用万法与调查/推荐摄入量
1、常见使用方法
(1)食品 未查见相关文献资料。
(2)保健食品 未查见相关文献资料。
(3)其他 腺苷和腺嘌呤可作为药品[11]。
2、调查/推荐摄入量
(1)调查摄入量 未查见相关文献资料。
(2)推荐摄入量 腺苷作为药品时:起始剂量:6mg快速静脉注射(1~2s)。重复给药:如果室上性心动过速未在起始治疗后的1~2min起效,可重复给予12mg的快速静脉注射。如需要可再次给予12mg的快速静脉注射。儿科用量要根据患儿的体重调整,体重低于50kg患者,起始剂量为0.05~0.1mg/kg快速静脉注射,如果PSVT仍未缓解则重复剂量可改为每次增加0.05~0.1mg/1kg,两次静脉注射之间注射生理盐水。最高剂量为0.3mg/kg,直到恢复窦性心律。对体重大于50kg的患儿可以按照成人剂量使用,但不推荐高于12mg。
七、国际组织和各国政府评价、批准、认可情况
中国 批准腺苷作为原料药和注射药品使用。
美国 FDA批准腺苷注射液作为快速静脉注射用药,属于血管扩张药、抗心律失常药、镇痛药和心脏药物(ATC:C01EB10)[101。GRN NO.000145.S-腺苷甲硫胺酸于1997年被FDA确认为新资源食品。
欧盟 未对腺苷和腺嘌呤进行评价。
澳/新 未查见相关文献资料。
其他 加拿大健康署批准腺苷用于PSVT时窦性心律的恢复,包括其他通路的传导受阻如Wolff-Parkinson-White综合征,还作为宽或窄QRS波患者的诊断工具。
八、注意事项和禁忌
不适宜人群 未查见相关文献资料。
禁忌 腺苷过敏者[8]。
与药物相互作用 很多心脏用药对静脉腺苷有抑制作用,如奎尼丁、β受体阻断药、钙通道阻断药、血管紧张素转换酶抑制药。但地高辛和维拉帕米(心室纤颤药物)很少影响腺苷的作用。甲基腺嘌呤,如咖啡因和茶碱能够竞争性拮抗腺苷的作用,而冠状动脉扩张药物双嘧达默能增强腺苷的功能[8]。
其他 腺苷的副作用(潮红、气急、胸痛)较常见,但多为一过性(1~2min内消失)。
九、小结
腺苷是一种内源性核苷酸,广泛存在于人体和动物体组织细胞中。腺嘌呤是存在于大多数生物体内的四种含氮碱基之一。用于分析腺苦的方法有高效液相色谱法(HPLC)、HPLC-MS、薄层色谱-紫外分光光度法等,腺嘌呤的分析方法包括化学修饰电极方法、化学发光方法、吸附溶出伏安法等。腺苦对心血管系统和其他系统及组织均有生物学作用,腺嘌呤具有植物激素作用和镇静、降血清胆固醇、抗缺氧等功能。腺苷的副反应主要为心律失常、惊厥等。
参考文献
[1] Huang L, Guo F, Liang Y, et al. Simple and rapid determination of adenosine in human synovial fluid with high performance liquid chromatography-mass spectrometry. Journal of Pharmaceutical and Biomedical Analysis, 2004, 36(4):877-882.
[2] 毛丽珍,阙沛红.虫草-中华束丝孢中腺苷的含量测定.中草药,1993,24(9):467.
[3] Tao Guo, Yi Sun, Yin Sui. et al. Determination of ferulic acid and adenosine in Angelicae Radix by micellar electrokinetic chromatography. Analytical and Bioanalytical Chemistry, 2003, 375(6):840-843.
[4] Tzeng H, Hung C, Wang J, et al. Simultaneous determination of adenosine and its metabolites by capillary electrophoresis as a rapid monitoring tool for 5'-nucleotidase activity. Journal of chromatography, 2006, 1129(1):149-152.
[5] Zen J, Chang M, Ilangovan G. Simultaneous determination of guanine and adenine contents in DNA, RNA and synthetic oligonucleotides using a chemically modified electrode. Analys. 1999, 124:679-684.
[6] Kuroda N, Nakashima K, Akiyama S. Chemiluminescence method for the determination of adenine after reaction with phenylglyoxal. Analytica Chimica Acta, 1993, 278(2):275-278.
[7] Farias P,Wagener A, Castro A. Ultratrace determination of adenine in the presence of copper by adsorptive stripping voltammetry. Talanta, 2001, 55(2):281-290.
[8] http://www.drugs.com/pro/adenosine.html.
[9] http://www.chemdrug.com/msdsinfo.asp?id=1413.
[10] http://www.souku.com.cn/viewFrame.jsp?toUrl=pay.jsp?url=3762620.
[11] http://www.mongabay.com/health/medications/Adenosine.html.